|
 |
| Kalp Yetersizliği Elektronik Haber Bülteni Yıl: 1 Sayı: 3 / 2008 |
Geçmiş anket sonuçları Bülten İstek Formu |
Acute viral myocarditis. Eur Heart J 2008;29,2073–82. Prof. Dr. Metin Özenci
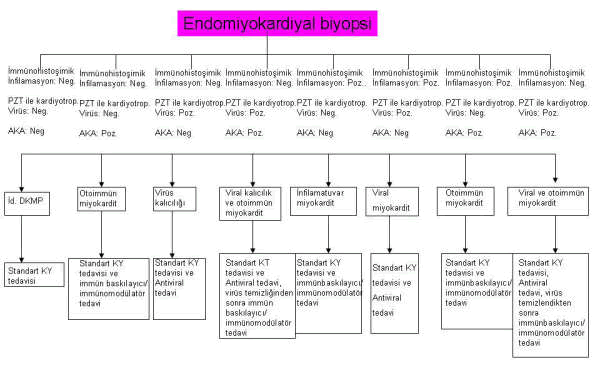
Miyokardit yapan kardiyotropik virüsler; Adenovirüs (ADV), enterovirüs (EV), Epstein-Barr virüsü, insan herpes virüsü 6 (HHV6), parvovirüs B19 (PVB19) ve sitomegalovirüs olup, HHV6 ve PVB19, 2008 yılı için en sık görülen nedenleri oluşturmuşlardır. Akut virüs infeksiyonu, genetik yatkınlık ile birleştiğinde miyokardit oluşabilir. Klinik ise asemptomatik olabileceği gibi fulminan veya kronik bir seyir izleyebilir. Asemptomatik tablo; kısmi veya tam iyileşmeyle sonuçlanabileceği gibi, DKMP ye de dönüşebilir. Fulminan tablo; ölümle sonuçlanabilir veya kısmi/tam iyileşebilir. Kronik olguların ise DKMP’ye dönüşme veya kısmi/tam iyileşme olasılıkları vardır. Akut miyokarditte, kardiyak semptomlar çıkmadan önce üst solunum yolu veya gastrointestinal yola ait soğuk algınlığı benzeri yakınmalar vardır. Günler veya haftalar içinde yorgunluk, nefes darlığı, atipik göğüs ağrısı, çarpıntı gibi kardiyak semptomlar ortaya çıkar. Fizik muayenede sinüs takikardisi, S1 yumuşaması, galo ritmleri, MY ve/veya TY üfürümleri, ender, ancak görüldüğünde patognomonik olan perikart frotmanıdır. Çoğu olguda sözü edilenler akut olarak ortaya çıktığından, hızla DKMP tablosu gelişen, idyopatik ventriküler aritmisi olan, kardiyovasküler kollaps’a giren, koroner arterleri normal olduğu halde EKG lerinde Mİ örneği olan olgular miyokardit kabul edilmelidir. Bu durumda da, akut viral miyokardit’in diğer infeksiyöz miyokarditler, Mİ, dev hücreli miyokardit, eozinofilik miyokardit, post/peripartum KMP ve kardiyak sarkoidoz’dan ayırt edilmesi gerekir. Virüsün miyokarda girişinden sonraki fizyopatolojik süreç ise 3 evrelidir. Birinci evre; virüs aracılı hücre erimesi (lizis) ile miyositin doğrudan yaralanmasıdır. Bu aşamada hücre yapıları ayrışır, hücre içine virüs girişi kolaylaşır, komşu miyositler tutulur ve kalp büyür. Bu evrede inisiyal hücresel ve hümoral bağışıklık yanıtı tablonun ilerlemesini engelleyebilir. İkinci evre; inisyal miyosit yaralanmasının tetiklediği bağışıksak düzensizlik (immün disregülasyon) nedeniyle miyokardın otoimmün nedenli yaralanmasıdır. İlk evrede engelleyici etkisi olabilen inisiyal hücresel ve hümoral bağışıklık yanıtı, bu evrede yıkıcı etkiden sorumludur. Ayrıca (akut rumatizma karditinde olduğu gibi) vral ve kardiyak doku molekülleri arasındaki benzerlikler de otoimmün sürecin gelişmesine katkıda bulunurlar. Üçüncü evre; Hücre içi kardiyak proteinlerin salımının, T hücre aktivasyonunun, sitokin salımının, matriks parçalayıcı proteazların salımının görüldüğü ve miyokardın yeniden şekillenmesiyle DKMP tablosunun geliştiği dönemdir. Bu fizyopatolojik süreçte KY’ne doğru ilerleyen bir miyokardit tablosu için aydınlatılamayan 2 nokta vardır. İlki; fulminan miyokarditte kimi olguların ölüp kiminin tamamen iyileşmesinin nedeni, ikincisi de; sözü geçen kardiyotropik virüslerle insanların %90’ının yaşamlarının herhangi bir evresinde karşılaşmalarına karşın neden pek azında miyokardit geliştiğidir. Birinci soruyu yanıtlamaya yönelik postülata göre; fulminan miyokardite karşı verilen ve virüsü yok etmeye yeterli orandaki aşırı infilamasyon miyokartta geçici bir afallama ve işlev bozukluğuna yol açmasına karşın, olguyu ikinci evreye sokmadan klinik tabloyu düzeltebilir. Yeterli infilamasyon yanıtı üretemeyen (sub)akut olgular ise ikinci evreye geçerek kronik otoimmün infilamasyon ve tam olmayan bir klinik iyileşme ile yaşamlarına devam ederler. İkinci sorunun yanıtı ise olasılıkla genetik temel ile ilgilidir. Örneğin coksaki B3 infeksiyonunda distrofin gen mutasyonu olanlarda miyokardit ve KY gelişimi kolaylaşmakta; viral proteazlarla distrofin ve/veya sarkoglikan çözülmesi olanlarda ise miyokart yaralanması görülmektedir. Miyokardit kuşkusu doğduğunda tanı için izlenmesi gereken yol ise şöyledir; Ayrıntılı anamnez, EKG ve kardiyak enzimleri, serumda antikalp antikor varlığını da içeren kan testleri alınmalı; ekokardiyografi ve gerekiyorsa kardiyak MR’ı da içeren görüntüleme yöntemleri uygulanmalıdır. İlk 48 saat içinde olguların neredeyse %57’sinde kendiliğinden düzelme olmasına karşın, kalp işlevinde ilerleyici bozulma gözlenenlerde koroner anjiyografi (KAG) yapılmalı, koroner arter hastalığı dışlanıyorsa tanısal amaçlı EMB alınmalıdır. 48 saatten sonra kalp işlevinde bozulma bulguları sebat edenlere de aynı uygulamalar yapılmalı, kendiliğinden iyileşenler ise en az 3 yıl izlenmelidir. D’Ambrosio ve ark.na göre DKMP’ye dönüşenlerin oranı %14-52 dir. 3-5 yıl sağkalım oranı %56-83 dür. Akut fulminan miyokardit de ölümden kurtulanlarda 11 yıl sağkalım oranı %93 bulunmuştur. Akut ancak fulminan olmayan miyokarditlerde bu oran %45 dir. Kuhl ve ark. göre Miyokartta virüsün sebat ettiği olgularda, sol ventrikülde ilerleyici bozulma gözlenirken; viral genom temizliği sağlanan olgularda sol ventrikül işlevi önemli oranda düzelmektedir. Akut miyokardit olgularında %20 dolayında olan 1 yıllık mortalite oranının başlangıçtaki azalması, izleyen 3 yılda stabilize olur. İyileştiği varsayılan çoğu olguda tekrarlama riski olduğundan, olguların 3 yıl veya daha fazla izlenmesi tavsiye edilmektedir. Artık sıra EMB örneği alınan olgularda gerçekten miyokardit var mı? Varsa tedavide kime? Hangi? yol izlenmeli sorusuna geliyor. 1987 de önerilen Dallas sınıflandırması, miyokarditlerin tanısal ölçütlerini standardize etmek amacına yönelik girişimlerin içindeydi. Ne var ki, patolojik yorum farklılıklarına ve örnekleme hatalarına açık olması; patolojik bulguların gerçek nedeni hakkında bilgi vermemesi gibi eksiklikleri vardı. Otoimmün miyokarditlerde inflamasyon varlığını kanıtlayacak immün boyama tekniklerini veya viral miyokarditlerde yapılması gereken polimeraz zincir tepkimesi (PZT) yöntemlerini içermemesi nedeniyle günümüzde otoimmün ve viral miyokarditlerin tanısında altın standart olarak kullanılabilme özelliği kalmadı. Bu nedenle, viral ve otoimmün kalp hastalıklarının yeniden tanımlanmalarına yönelik son çabalar deyim yerinde ise “ Dallas kriterlerinin ölümü” ile sonuçlandı. Günümüzde miyokardit tanısı için altın standart, 1995 WHO kardiyomiyopati sınıflandırımına göre EMB örneklerinden ışık mikroskopisiyle histolojik Dallas kriterlerinin sorgulanması, ancak yeni immünohistoşimik yöntemlerin, in situ hibridizasyon’un ve PZT’in de araştırmaya eklenmesiyle ulaşılacak bilgilerin birlikte değerlendirilmesidir. Daha sonra immünohistoşimik yöntemlerle infilamasyon’un; PZT yönteminin de kardiyotropik virüs’ün varlığı veya yokluğu hakkında vereceği bilgiler, serumda kalbe karşı antikor varlığının da göz önüne alınmasıyla birlikte değerlendirilerek aşağıdaki tabloda özetlenmiş olan 8 değişik tedavi seçeneği öneriliyor.
|
| 2008 - 2024 © Bu sitenin tüm hakları Türk Kardiyoloji Derneğine aittir. |